Diseñan moléculas para tratar enfermedades neuronales
A partir de una toxina del
potente veneno del caracol de mar Conus geographus, se propondría un fármaco
para controlar este tipo de afecciones. Dos péptidos (cadenas de aminoácidos)
diseñados ofrecen resultados promisorios.
Después de adelantar un
complejo trabajo de 80 ensayos in silico (virtuales), como parte de una tesis
doctoral, el profesor Édgar Reyes y el estudiante de Maestría en Ciencias
Bioquímicas, César Machuca, guardaron en un tubo de ensayo el resultado de sus
estudios.
En ese ligero equipaje
científico, que llevaron a la Universidad de Nueva York, iban en forma
liofilizada (sólida, sin solventes) todas las expectativas de 15 años de
trabajo en la Universidad Nacional de Colombia (UN): un tipo de moléculas
denominadas péptidos (cadena de aminoácidos), diseñadas para actuar sobre una
proteína específica, que podrían servir para tratar enfermedades neuronales,
como isquemias, párkinson o alzhéimer.
Si estos péptidos funcionan,
podrían evitar el daño neuronal producido después de una isquemia cerebral o
trombosis, como se conoce esta patología, al actuar en calidad de agentes
reguladores para que las células alteradas (cuando falte el oxígeno y nutrientes)
retornen a la normalidad. Tal aplicación resulta muy valiosa, pues aunque es un
modelo inicial sobre el que se desarrollan ensayos in vitro (de laboratorio),
también funcionaría en otras alteraciones neuronales.
En el micromundo de los
péptidos, hallar los indicados para esta función tan compleja y precisa es la
tarea titánica en la que se ha embarcado el Grupo de Investigación en Proteínas
(GRIP) de la UN, del cual forma parte el profesor Reyes, doctor en Ciencias
Químicas.
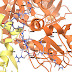
IMÁGENES: Edgar Reyes
Para ello, este equipo de
investigación parte de un receptor de glutamato a nivel neuronal, llamado NMDA
(N–Metil–D–Aspartato). El glutamato es
uno de los neurotransmisores más importantes del sistema nervioso
central, porque interviene activamente en la transmisión de las corrientes
eléctricas que producen procesos fisiológicos tan fundamentales en el ser
humano, como la memoria y el aprendizaje. Además, estos requieren canales
iónicos, complejos proteicos con un poro que permite la entrada selectiva de
varios iones a una célula.
Cuando estos canales no
funcionan de forma adecuada generan desbalance entre las neuronas y afloran
algunas patologías como dolores neuropáticos, alzhéimer, isquemias o párkinson.
La isquemia, el modelo sobre
el cual trabaja el GRIP, se produce cuando el aporte de oxígeno al encéfalo
disminuye o es interrumpido, según el profesor Rodrigo Pardo, de la Facultad de
Medicina de la un.
“Al haber bloqueo en el
transporte de oxígeno a las células, la reacción puede llevar a la muerte
neuronal”, explica por su parte el profesor Reyes. Además, precisa, el mayor
impacto no es generado por el evento isquémico, sino por el fuerte choque que
sufren las células al restablecerse el flujo sanguíneo, pues estas reaccionan y
abren todos sus canales, lo cual produce una entrada excesiva de calcio. Así,
esto generaría más daño que el mismo derrame cerebral.
Por ello, un complejo
proteico como el receptor NMDA, según el doctor Reyes, es un buen blanco
farmacológico para estos casos, ya que contribuiría de manera eficaz en la
respuesta de las células ante el restablecimiento del flujo sanguíneo en
condiciones más regularizadas y, como tal, menos nocivas.
La toxina del caracol
Para iniciar el diseño de
los péptidos, que se unieron al canal iónico deseado, el equipo investigador
tomó como base de estudio una toxina denominada Conantokina G, extraída del
Conus geographus, un caracol de mar de vistosos colores.
Conus Geographus, la especie de caracol marino de la cual se
obtuvo la toxina Conantokina G,
base del estudio del Grupo de Investigación en Proteínas (GRIP).
base del estudio del Grupo de Investigación en Proteínas (GRIP).
Este molusco, según el
biólogo Juan Manuel Díaz Merlano de la un, es una especie de gasterópodo de la
familia de los cónidos, a la cual pertenecen alrededor de 500 especies, la
mayoría de ellas localizadas en mares tropicales, en especial, arrecifes de
coral. “Se trata de una especie común y como tal no figura en las listas rojas
de especies amenazadas”, puntualiza.
El profesor Díaz indica que,
como todos los cónidos, es una especie carnívora. “Su alimento son los peces,
que caza mediante un dardo en forma de arpón,
acoplado con una glándula que
produce uno de los venenos más potentes entre organismos marinos, el cual puede
causarle la muerte al ser humano”.
Al respecto, explica, la
letalidad del veneno radica en que son animales de movimiento muy lento y se
alimentan de peces de desplazamiento rápido. “Cuando el pez es alcanzado por el
dardo, el veneno actúa inmediatamente para impedir que el animal escape y
termine en la boca de otro pez o pulpo”.
Esta toxina tendría la
capacidad de bloquear el paso excesivo de iones a través del canal de estudio,
pues se une de manera muy selectiva a la subunidad que modula la apertura o
cierre del receptor evaluado, explica el profesor Reyes. Una subunidad es una
parte del complejo proteico. En otras palabras, el complejo es una asociación
de varias proteínas (subunidades) que unidas permiten que funcione, en este
caso, como canal iónico.
La sustancia tóxica
seleccionada funciona como antagonista del receptor, toda vez que cambia su
acción normal y bloquea el paso de iones a través de este. Con ella han
desarrollado ensayos en el mundo, estos indican que se une muy fuerte a la
subunidad y casi bloquea el canal de manera permanente. Sin embargo, en casos
como los mencionados, se requiere que el bloqueo sea solo temporal para
asegurar que estos canales vuelvan a ser funcionales.
Por tanto, los
investigadores de la un trabajan en el diseño de péptidos que tengan una
afinidad menos fuerte que la Conantokina G, con el fin de lograr su
reversibilidad al suministrarlos después de un evento isquémico y, así, evitar
el daño neuronal. El secreto está en disminuir gradualmente su efecto o lograr
que este sea reversible y retirar el péptido para que la célula siga
funcionando de manera natural.
Bioinformática, laboratorio
virtual
Tales cadenas de aminoácidos
fueron diseñadas con ayuda de la bioinformática, que permite simular su
comportamiento in silico, un procedimiento virtual que resulta muy favorable,
pues no requiere trabajo in vitro, ni in vivo (pruebas de campo), realizado con
animales de experimentación. “Con ella se simulan las interacciones o uniones
entre los péptidos y el receptor”, precisa el investigador Reyes. Esta parte
del proyecto fue financiada por Colciencias.
La bioinformática
proporciona herramientas especializadas que facilitan simular las interacciones
de cada uno de los péptidos propuestos con la subunidad en estudio, con el fin
de realizar un análisis exhaustivo que permita seleccionar aquellos con mejores
probabilidades de funcionamiento, de acuerdo con el diseño realizado.
En principio, fueron
propuestos 80 péptidos y después del análisis in silico determinaron evaluar in
vitro cuatro de ellos y uno adicional que actúa como control. Posteriormente,
fueron llevados liofilizados a Nueva York para los estudios correspondientes.
A la fecha se han examinado
dos péptidos y el control. En desarrollo de la tesis doctoral en Biotecnología
del estudiante Edwin Reyes, calificada como meritoria, fue evaluada la
especificidad de cada uno de los péptidos hacia el receptor NMDA y la
reversibilidad de su unión al disminuir su concentración en el medio.
Por medio de la técnica de imagen de calcio (Calcium
Imaging) se determina la viabilidad de las células antes y después de
someterlas a una deprivación de glucosa y oxígeno (modelo de isquemia). A la
izquierda están las células en el campo que se está evaluando y a la derecha
aparece la medición de respuesta de cada una de ellas ante un estímulo
eléctrico. Si hay respuesta, la célula es viable.
El investigador dispuso los
péptidos en cultivos celulares y con la técnica de electrofisiología (estímulos
eléctricos) revisó si los canales funcionaban o actuaban como antagonistas;
además, si no quedaban adheridos al receptor. Por ello, fue necesario hacer la
evaluación durante la presencia del péptido en el medio y luego de ser
retirado, para determinar la recuperación de las células.
Al final, se encontró que
dos de estos péptidos funcionan muy bien al ejercer la función de antagonista
buscada y, además, actúan de manera selectiva para la subunidad GluN2.
Dado el importante hallazgo,
el equipo inició el trámite de patentar los péptidos junto con un tercero que
se potencia como agonista del receptor, es decir, con características similares
a los dos primeros, pero sin efecto de bloqueo. Se quería como un control
negativo, que no le hiciera nada. Pero el efecto fue contrario a los otros dos,
es decir generaba efecto, pero de agonista, con lo que al adicionar este
péptido, el receptor funciona como si estuviera con su ligando natural (glutamato).
Sobre los dos péptidos
antagonistas, analizados según la técnica de imagen de calcio (calcium
imaging), fue recopilada tanta información, que tuvo que ser almacenada en un
disco de un terabyte (un trillón de bytes).
Por lo pronto, la
investigación, en la que ha colaborado el profesor John Sutachán, de la
Universidad Javeriana, quien facilitó el contacto con la doctora Esperanza
Recio–Pinto, de la Universidad de Nueva York, tiene pendiente cuatro pruebas
concluyentes.
Una vez inicien las pruebas
in vivo se propondrá un fármaco que permita controlar enfermedades neuronales.
Por ejemplo, solo en el caso de la isquemia cerebral, están asociadas en forma
directa a 6.2 millones de decesos anuales, que representan el 10.6 % de la
mortalidad mundial, registra la Guía de práctica clínica para el diagnóstico,
tratamiento y rehabilitación del episodio agudo del ataque cerebrovascular
isquémico en población mayor de 18 años, dirigida por el profesor Pardo.
En Colombia, señala el
documento, la prevalencia de esta enfermedad, según edad y género, fluctúa
entre 1.4 a 19.9 casos por cada 1.000 habitantes. Por ello, estos estudios,
como el que realiza el GRIP, constituyen una de las más esperadas respuestas
para el mundo médico y millones de pacientes.